Реакционная способность в реакциях радикального присоединения к ненасыщенным соединениям
Термохимический аспект
Начнем анализ радикального присоединения с термохимического аспекта. Хотя радикальное присоединение в большинстве случаем имеет низкий барьер активации и, следовательно, ранее ПС, возможность существования связи между свойствами ПС и продуктов обсуждалась давно. В качестве объяснения приводится факт, что из-за спин-поляризации (а она начинается на ранних стадиях реакции), ПС и продукт имеют сходное электронное строение.
В Таблицах II и III приведены некоторые энтальпии реакций (ΔΔHf) и барьеры активации (ΔΔH≠f). Первое очевидное заключение –β-присоединение предпочтительнее во всех рассмотренных случаях, в среднем на 5 ккал/моль. Такое различие может быть объяснено как термохимически (образуется вторичный, а не первичный радикал), так и стерически (более доступен реакционный центр, меньше деформация в ПС). Как видно из Рис. 1, во всех рассмотренных реакционных сериях “радикал → мономеры” существует практически линейная корреляция между энтальпией реакции и активационным барьером (этакий вариант корреляции Поляни–Семенова). Точки, представляющие β-присоединение (нижняя группа точек), примыкают к корреляционным прямым более плотно.
Таким образом, мы можем констатировать, что расчетная энтальпия реакции радикального присоединения к C=C являются индексом реакционной способности практически той же "силы", что и расчетный барьер активации для газофазного присоединения.
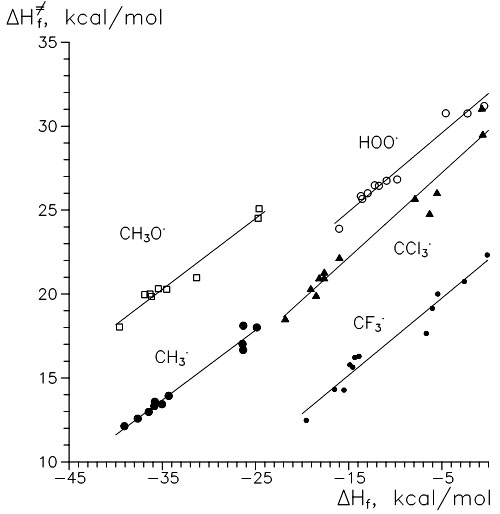 Рисунок 1. Соотношение между расчетными энтальпиями реакций и соответствующими барьерами активации.
Рисунок 1. Соотношение между расчетными энтальпиями реакций и соответствующими барьерами активации.
HOO–CH2–CHX• | HOO–CHX–CH2• | |||
|---|---|---|---|---|
| ΔΔHf | ΔΔH≠f | ΔΔHf | ΔΔH≠f | |
| Eth | −11.76 | 26.44 | ||
| Prop | −13.71 | 25.83 | −4.59 | 30.77 |
| St | −18.82 | 23.00 | — | — |
| AN | −12.97 | 26.01 | −2.26 | 30.76 |
| MA | −10.94 | 26.75 | −0.47 | 31.20 |
| VA | −16.03 | 23.89 | −9.81 | 26.83 |
| VCl | −12.21 | 26.48 | −9.87 | 30.15 |
| VCl2 | −13.55 | 25.67 | −5.98 | 32.03 |
CH3–CH2–CHX• | CH3–CHX–CH2• | |||
|---|---|---|---|---|
| ΔΔHf | ΔΔH≠f | ΔΔHf | ΔΔH≠f | |
| Eth | −34.32 | 13.93 | ||
| Prop | −35.80 | 13.58 | −26.32 | 18.12 |
| St | −41.68 | 11.44 | ||
| AN | −36.46 | 12.98 | −26.40 | 17.02 |
| MA | −35.04 | 13.44 | −24.86 | 18.01 |
| VA | −39.08 | 12.13 | −26.34 | 16.67 |
| VCl | −35.87 | 13.32 | −30.99 | 16.90 |
| VCl2 | −37.64 | 12.58 | −27.50 | 19.61 |
